【新唐人北京時間2026年03月19日訊】前15篇,我們揭開了進化論發跡的造假之路:「爪哇猿人」(Java Man)是相距45英尺的「猿頭蓋+人股骨」湊成的,「爪哇猿人Ⅱ」是漫山遍野湊的頭骨殘片,皮爾當「曙光猿人」(Eoanthropus)欺騙41年才被拆穿,美國「黃昏猿人」(Hesperopithecus)招搖5年被曝光,竟是野豬!
著名的「北京猿人」,隱匿枕骨大孔數據,借智人的人型腿骨才能直立起來,成為「猿人」。9個致命問題和朊病毒,否定了它們自相殘食,只能是被人捕食的獵物,不是人祖。隨之,以「北京人」為基礎的中國猿人歸於錯誤。
北京猿人之後,進化論的里程碑事件,就是米勒實驗推出的化學進化假說,卻是建立在21個錯誤假設基礎上的,本文繼續闡釋。
132. 誰污染了米勒的樣品?
前面講到:複檢1958年米勒實驗模擬火山噴發氣體的化學進化,「進化出」(生成)的天冬氨酸、谷氨酸、絲氨酸明顯被細菌污染了[1],胺基酸的左手型,大大高於右手型。因為非生物製造、純化學反應生成的胺基酸,左手型和右手型均等,而生物蛋白質胺基酸都是左手型的。而AI回答,卻給出了沒有被污染的假結果。
這個污染,是米勒(Stanley Lloyd Miller)自己造成的?還是產物存放五十多年造成的?
如果是過久存放造成的,後人的檢測實驗就毫無意義,檢測污染物幹啥?後人不會打自己的臉。2008年研究米勒實驗產物的論文[2],沒發現樣品污染,不等於沒污染。2011年發表的論文揭示了污染,有實驗數據,表明一定有污染。
「米勒於2007年5月20日逝世。因其開創了生命起源的實驗研究時代,本研究謹以此文紀念其貢獻[1]。」2011年論文本是為紀念米勒的貢獻而寫,結果卻揭了祖師爺的短。
為什麼能肯定是米勒自己污染的呢?因為:
(1)如果是五十多年存儲造成的污染,所有樣品在相同的存儲條件下,都會被污染,不會只發生在幾種胺基酸上;
(2) 米勒實驗中,不斷取樣,不斷製造污染的機會;
(3)米勒完成製造胺基酸的實驗後,據文獻[1]引用的實驗記錄,把產物(黑湯)用陽離子交換法,進一步分級分離(還有相應的參考文獻[3]),再經蒸發乾燥,成為乾燥物,分別編號。都是在有菌環境下接受污染。
(4)放入滅菌玻璃瓶中保存,只在長期存放時考慮了細菌污染,用了滅菌瓶。
133. 取樣是單向閥門,不會造成污染!?
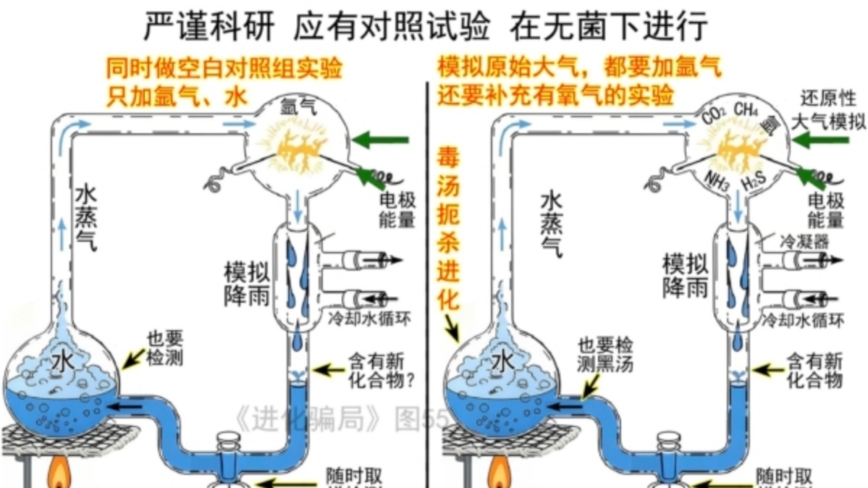
「米勒實驗取樣是單向閥(置頂圖下方),液體只出不入,不會造成污染。」 一位研究生這樣反饋。
這就是和米勒-尤里相同的「半外行的思維」,沒做過微生物製藥方面的實驗。只要接觸空氣就會被細菌污染。上圖單向閥一拉起來,上下兩個磨砂面一遇到空氣,就很可能碰上細菌,碰上一個就會污染,在這個含有機物的水循環內生長繁殖。從左方冷凝模擬降雨,到進入加熱燒瓶這一段,是很適合一般細菌繁殖的。
既然米勒實驗開始就有污染的大漏洞,後面的結果就不可信了。
134. 米勒實驗,全程污染
米勒對實驗終產物(黑湯)的收集、分離胺基酸的過程,都暴露在空氣中,但是污染並不嚴重。因為溶液蒸發獲取乾燥物,細菌在乾燥環境下,無法生長、增殖,微量的細菌污染不會再增加——污染的主要階段不在這裡,在生產環節。為什麼?
因為如果是後續純化中污染的細菌,細菌的各種「左手胺基酸」分子,會均勻分布,而不是只污染產量低的天冬氨酸、谷氨酸、絲氨酸,高產量的其它胺基酸的也會被細菌的左手型胺基酸污染。所以,關鍵在生產環節。
那為什麼高產量的那些胺基酸,沒有被污染呢?其實也污染了,而且是生產環節污染的,看下圖。
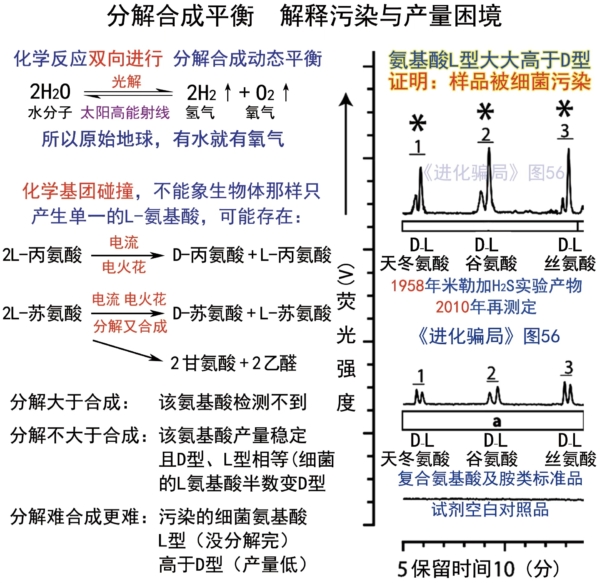
(1)為什麼賴氨酸、祖氨酸、精氨酸,至今沒在實驗室裡「進化」出來?
——理論上原子基團隨機碰撞,一定能碰出它們來,沒檢測出它們來,可能是它們在這樣環境下的分解太快,大於合成速度。
(2)甘氨酸、蘇氨酸等產量高的胺基酸分子,D型、L型在誤差範圍內相等,是沒被污染嗎?
——不是,也同時被細菌的左手L-胺基酸污染了。只是因為這些胺基酸分子的生成速度,不小於分解速度。所以細菌的L胺基酸,在不斷分解與生成的動態平衡中,變成均等的L、D兩種胺基酸,L胺基酸高含量被分解掉了。
(3)為什麼上圖右,只有天冬氨酸、谷氨酸、絲氨酸的L型大大高於D型?
——可能是細菌的這三種胺基酸,在該反應器中,分解速度低,沒分解完有殘留,而且合成產量低,這樣細菌L胺基酸的優勢,就顯現出來了。
上圖右的低產量胺基酸的L型峰高,只有在生產環節的「分解合成動態平衡」中才能實現,表明是在生產環節發生的污染。
135. 分解合成動態平衡,否定化學進化
上面的化學反應「分解-合成動態平衡」,不是我們發明的假說,而是實實在在的化學反應的現象,早就寫進化學教科書裡的!只是我們用來解釋了米勒實驗的幾個困境。
如果真是這樣,那麼:
(1)這樣的「原始大氣」條件下,化學進化永遠不能實現,因為分解大於合成的賴氨酸、組氨酸、精氨酸永遠造不出來。除非換反應條件。
(2)這還沒加入紫外線呢。紫外線對胺基酸分子、蛋白質分子破壞性更大,這樣自然條件下,胺基酸分子的產量更低,更無法化學進化了。
(3)合成分解達到平衡後,胺基酸的產量永遠上不去,無法達到後續反應所需的高濃度,也就否定了化學進化假說。
所以,當今用新技術,高效液相色譜-質譜連動檢測出微量胺基酸,就以為大功告成,恰恰是大功告吹!因為那麼低的濃度,達到平衡後也不再增加了,不再累積了,無法繼續了。
136. 米勒實驗還有漏洞,成了細菌培養器?
米勒實驗還有一個大漏洞,現今學術界已經承認了,就是用了硼硅酸鹽玻璃器(酸性),會被鹼性氣體氨氣腐蝕,造成玻璃表面產生很多粗糙的坑洞,增加了表面積。一些學者的實驗表明,用不耐腐蝕的聚四氟乙烯替換玻璃容器管道,產生的有機物就少得多[4]。
上圖右下方溫度適宜細菌生長的玻璃管裡,腐蝕產生的大量微坑洞,表面粗糙的,細菌能附著在那裡,在一定程度上,免於被循環水帶入加熱反應池(帶入也不會被殺滅盡),在微坑裡,在循環的含有機分子的水中生長、繁殖!
這個漏洞,讓米勒實驗的右下方部分,成了細菌培養器。雖然結果表明是微量污染,但是至少成倍地影響了幾種胺基酸的測定結果,也使著名的、劃時代的米勒實驗,結果不太可信了。
137. 錯誤15,假設蛋白質的20種胺基酸,都能這樣進化出來
化學進化的實驗至今已經72年,米勒和後來者想盡了各種辦法,賴氨酸、祖氨酸、精氨酸,還是沒在實驗室裡模擬「自然條件下產生出來」。現在我們知道了,所謂「模擬自然條件」,都不自然,自然界沒有那樣的反應濃度、能量和抗毒素機制。
138. 錯誤16,假設胺基酸能長期保存,用於後續進化
這是絕無可能的。胺基酸容易分解,蛋白質分子更容易被破壞,特別在毒素、紫外線、加熱的環境下。就算幻想真的「進化出一個長鏈大蛋白分子」,在米勒實驗裝置的循環加熱下,電擊下,也會失活,進化又完了!
139. 錯誤17~18,檢測「調包」,偷梁換柱
錯誤17,假設上圖取樣瓶內的檢測物A,就是持續加熱燒瓶內的終產物B。取樣瓶內的溶液是蒸餾後的、清澈的,而加熱燒瓶內是發黑的湯,檢測的清澈溶液再回流到黑湯內,會被破壞掉,故意不檢測?也就是說,米勒實驗檢測的,並不是實驗1週後的終產物,偷梁換柱了!類似「魔術」技巧。
錯誤18,假設實驗一週後的產物,不用再檢測——那才是終極產物,那才是留下來進行化學進化的——那些發黑的湯不檢測?怕檢測出惡果嗎?這也是米勒實驗最不合理的地方之一。
米勒從1952年實驗,到2007年逝世,55年都沒檢測那些發黑的終產物——那可是進化論幻想的「地球生命誕生的搖籃」、「孕育一切生命祖先的聖水聖湯」!為啥不檢測呢?也可能早就檢測了,因為結果不理想,隱藏了——不管怎麼樣,都不是科學的態度。
140. 嚴謹的生物實驗,應該這樣設計
(1)因為是模擬原始地球,那時連細菌還沒有,所以必須全在無菌環境下進行。又因為胺基酸產量是微量的,所以微量細菌的胺基酸足以干擾反應結果,因此更要無菌。
(2)必須做對照組實驗。不會做對照,生物學就沒入門。這個對照實驗,本文開頭實驗裝置圖左,充入氬氣做空白,因為氬氣是惰性氣體,不發生化學反應,而且在當今大氣層中,氬氣的含量是米勒所有假說氣體總合的30倍以上!所以要用氬氣。右邊的反應裝置,加甲烷、氨氣、氫氣,也要加些氬氣。
左右兩套相同的設備,同時走一個完整的實驗流程下來,結果再對比。空白對照實驗,產物分析沒見胺基酸產生,才能證明沒有本底污染,否則,就得找出污染源,再繼續實驗。
有對照實驗,生物實驗的結果才有可信度。從這點上看,米勒的外行實驗,沒有可信度。
141. 進化論只認1點有漏,無視21點大錯
進化論者,只承認米勒實驗有1個疏漏,就是上面說的沒考慮「酸性玻璃會與鹼性氣體反應」,造成有機物產量偏高。進化論認為這是歪打正著,因為地球原始環境硅酸鹽岩石多,都能和氨氣反應,促進了進化!
而米勒實驗的21個基礎錯誤,雖然以前沒有這樣系統總結過,個別學者零散提出的,沒這麼系統這麼多,但是學術界還是全然不顧。不管三七二十一,只看那無窮小的概率可能性,無視無窮大的不可能性,依然追捧米勒實驗的劃時代偉大意義——選擇性失明,一葉障目不見森林,這就是進化論的傳統思維方法。
(未完,待續)
責任編輯:張憲義#
參考文獻:
1. Eric T Parker et. al. Primordial synthesis of amines and amino acids in a 1958 Miller H2S-rich spark discharge experiment. PNAS. 2011 Mar 21;108(14) doi:10.1073/pnas.1019191108
2. Johnson AP, et al. The Miller volcanic spark discharge experiment. Science. 2008;322:404. doi: 10.1126/science.1161527.
3. Christianson D, et. Al. Separation and determination of quaternary nitrogen compounds and other nitrogenous substances by ion exchange chromatography application to analysis of corn extracts. Anal Chem. 1960. (32):874–878
4. Criado-Reyes, et al. The role of borosilicate glass in Miller–Urey experiment. Sci Rep 11, 21009 (2021) doi: 10.1038/s41598-021-00235-4
(點閱《進化騙局》系列文章)
(轉自大紀元/責任編輯:李紅)